Knochenkrebs–Forschungslabor
Im Labor versuchen wir, die Biologie von Knochensarkomen besser zu verstehen, um neue therapeutische Strategien gegen diese aggressiven Krebsarten zu entwickeln.
Aggressive primäre Knochenkrebsarten wie das Osteosarkom und das Ewing-Sarkom treten in der Regel im Jugendalter auf. Diese Patientinnen und Patienten werden derzeit mit Polychemotherapie, Chirurgie und Strahlentherapie behandelt. In den letzten Jahrzehnten konnten klinische Studien, in denen diese Behandlungen kombiniert und optimiert wurden, die Überlebensrate dieser Patientinnen und Patienten stark erhöhen, stossen aber in der Regel an ihre Grenzen, wenn weitere therapeutische Verbesserungen erreicht werden sollen. Zudem sind die therapeutischen Optionen für Patientinnen und Patienten mit rezidivierenden und/oder metastasierenden Erkrankungen nach wie vor begrenzt und die langfristigen Folgen der derzeitigen Behandlungen sind nicht zu vernachlässigen. Daher werden dringend neue therapeutische Ansätze zur Behandlung dieser Patientinnen und Patienten benötigt.
Die Entwicklung von Sequenzierungsverfahren der «nächsten Generation» hat die Entdeckung wiederkehrender genetischer Veränderungen bei Krebserkrankungen ermöglicht, auch bei Osteosarkomen. Medikamente, die auf die Folgen dieser genetischen Läsionen abzielen, wurden und werden in grossem Umfang entwickelt und haben die Krebsbehandlung revolutioniert. Leider gehören die meisten wiederkehrenden Veränderungen, die bei diesen primären Knochenkrebsformen festgestellt wurden, zur Kategorie der derzeit nicht medikamentös behandelbaren Veränderungen. Im Lichte dieses Aspekts zielt unser Labor darauf ab, mithilfe modernster zellulärer und molekularer Ansätze alternative Behandlungsmöglichkeiten für diese Patientinnen und Patienten zu finden und zu entschlüsseln, wie Krebszellen metastasieren und Behandlungen trotzen. Mit diesem Ziel laufen in unserem Labor derzeit drei Projekte:
Erforschung synthetischer letaler Mechanismen bei Osteosarkomen als neue therapeutische Möglichkeiten

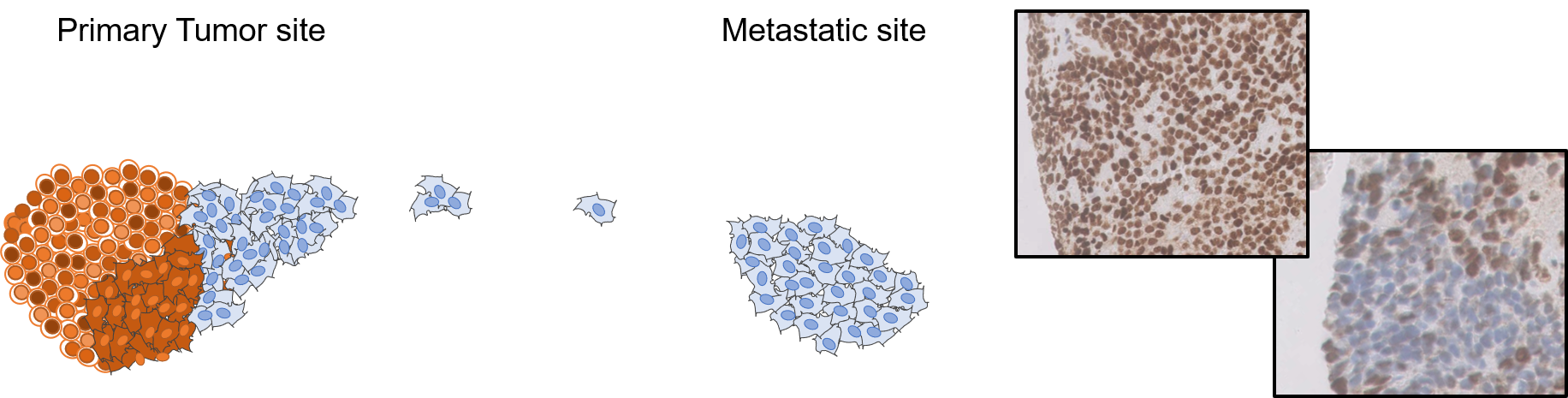
Da die meisten wiederkehrenden genetischen Ereignisse bei Ewing-Sarkomen zur Kategorie der medikamentös kaum behandelbaren Funktionsverluste gehören, zielen wir darauf ab, alternative zielführende Gene/Pfade zu identifizieren, um neue therapeutische Möglichkeiten für diese mutierten Krebsformen zu finden. Dazu verwenden wir genomweite und gezielte gepoolte CRISPR-Screening-Ansätze, um Kandidatengene zu identifizieren, die vorzugsweise mutierte Zellen (unten rot hervorgehoben), nicht aber Wildtyp-Zellen töten (Konzept der synthetischen Letalität).
Prävention und Erforschung von Metastasierungsmechanismen bei Osteosarkomen
Ewing-Sarkom-Zellen weisen eine starke Metastasierungsfähigkeit auf. Bei fast einem Viertel der Betroffenen sind zum Zeitpunkt der Diagnose bereits Metastasen vorhanden, was einen wesentlichen Faktor für die infauste Prognose bei diesen Patientinnen und Patienten darstellt. Die Mechanismen, die zur Metastasierung bei Ewing-Sarkomen führen, sind jedoch nur teilweise geklärt und sehr vielfältig. Ziel dieses Projekts ist es, den Ursprung und die räumlich-zeitliche Entwicklung besser zu verstehen, die diese Krebszellen zur Ausbreitung und zur Resistenz gegen die derzeitigen Behandlungen führen.
Von Betroffenen abgeleitete Modellierung von Osteosarkomen und Erstellung von Arzneimittelprofilen
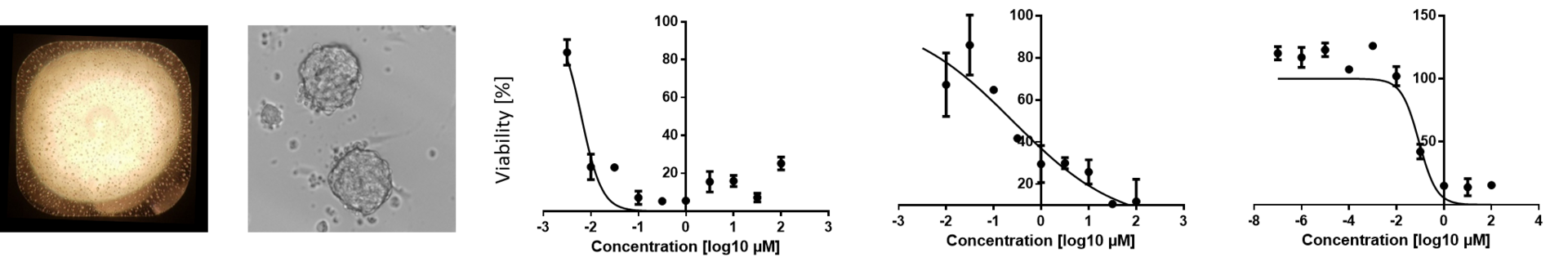
Das Bereitstellen zuverlässiger zellulärer Modelle für Osteosarkome ist von grösster Bedeutung, um das Ansprechen der Patienten auf die Behandlung vorherzusagen und ihre Biologie besser zu verstehen. In diesem an der Universität Zürich durchgeführten Kooperationsprojekt (Schwerpunktprogramm Klinische Forschung) wollen wir Plattformen der nächsten Generation zur Erstellung von Medikamentenprofilen für die klinische Anwendung bei Krebs entwickeln, Profile des Ansprechens auf Medikamente erstellen, um die Behandlung in Studien zu steuern, und mechanistische Erkenntnisse über diese Krebsformen gewinnen.
Ausgewählte Publikationen
- Surdez D, Zaidi S, Grossetête S et al. STAG2 mutations alter CTCF-anchored loop extrusion, cis-regulatory interactions and impact EWSR1-FLI1 activity in Ewing sarcoma. Cancer Cell. 2021;28:1535-6108(21)00208-7.
- Solé A, Grossetête-Lalami S, Surdez D et al. Unraveling Ewing sarcoma tumorigenesis originating from patient-derived Mesenchymal Stem Cells. Cancer Research. 2021.
- Surdez D, Landuzzi L, Scotlandi K, Manara MC. Ewing Sarcoma PDX Models. Methods Mol Biol. 2021;2226:223-242.
- Grünewald TGP, Cidre-Aranaz F, Surdez D et al. Ewing sarcoma. Nat Rev Dis Primers. 2018;4(1):5.
- Tirode F, Surdez D, Ma X et al. Genomic landscape of Ewing sarcoma defines an aggressive subtype with co-association of STAG2 and TP53 mutations. Cancer Discovery. 2014;4(11):1342-5.
Kontakt
Wir freuen uns über Ihre Kontaktaufnahme.

Prof. Didier Surdez
Leiter Tumorforschung
+41 44 510 74 22
E-Mail